Кальциевая сигнализация в т-лимфоцитах
Передача сигналов извне внутрь клеток осуществляется с помощью вторых мессенджеров. Этими ключевыми участниками клеточной сигнализации могут быть нуклеотиды, липиды, свободные радикалы или ионы. Все они связываются с определенными мишенями и вызывают последующие сигналы с определенной спецификой. Например, ионы имеют свойство вызывать быстрый ответ после индукции сигнала. Кальций является вездесущим вторичным мессенджером, который регулирует широкий спектр путей, таких как выживание клеток, пролиферация, активация, нейрогенез, движение клеток, сокращение мышц или передача сигнала через синапсы нейронов (Paemeleire et al, 2000; Berridge et al, 2000, 2003; Clapham, 2007; Grienberger & Konnerth, 2012; Humeau et al, 2018; Zumerle et al, 2019).
Кальций играет важную роль в активации Т-клеток. Эти лимфоциты представляют собой класс белых кровяных клеток, которые играют важную роль в адаптивном иммунном ответе, особенностью которого является наличие Т-клеточного рецептора (TCR) на их поверхности для обнаружения присутствия антигенов. В базальных условиях покоящиеся лимфоциты поддерживают внутриклеточную низкую концентрацию кальция (Vig & Kinet, 2009). Однако распознавание антигена TCR вызывает его активацию, характеризующуюся быстрым повышением уровня внутриклеточного кальция.
Активированные Т-клетки способны участвовать в иммунном ответе в соответствии со своим типом: цитотоксические Т-клетки (CD8+) уничтожают инфицированные клетки/патогены, хелперные Т-клетки (CD4+) активируют других участников иммунного процесса, регуляторные Т-клетки (Treg) предотвращают активацию аутоиммунных лимфоцитов, естественные киллерные Т-клетки (NKT) выделяют цитокины и лизируют антигенные мишени. Некоторые другие Т-клетки считаются "нетрадиционными", например, MAIT или γδ Т-клетки. Координация всех этих типов клеток необходима для успешного иммунного ответа.
Лимфоциты являются центральным компонентом механизмов иммунной защиты. Их активация является одним из ключевых шагов, необходимых для иммунного ответа. Исследовать это сложное физиологическое явление можно с помощью ратиометрической визуализации, отслеживающей кальциевые переходные процессы (Balagopalan et al, 2011). Этот метод может дать исследователям возможность улучшить понимание активации иммунных клеток и изучить патофизиологические нарушения.
Inscoper liveRATIO, современное и универсальное решение для ратиометрической визуализации
Inscoper liveRATIO - это комплексное решение для микроскопии с ратиометрической визуализацией. Продукт состоит из программно-аппаратного комплекса, совместимого с современными видеомикроскопами, используемыми в биологии (рис. 1).
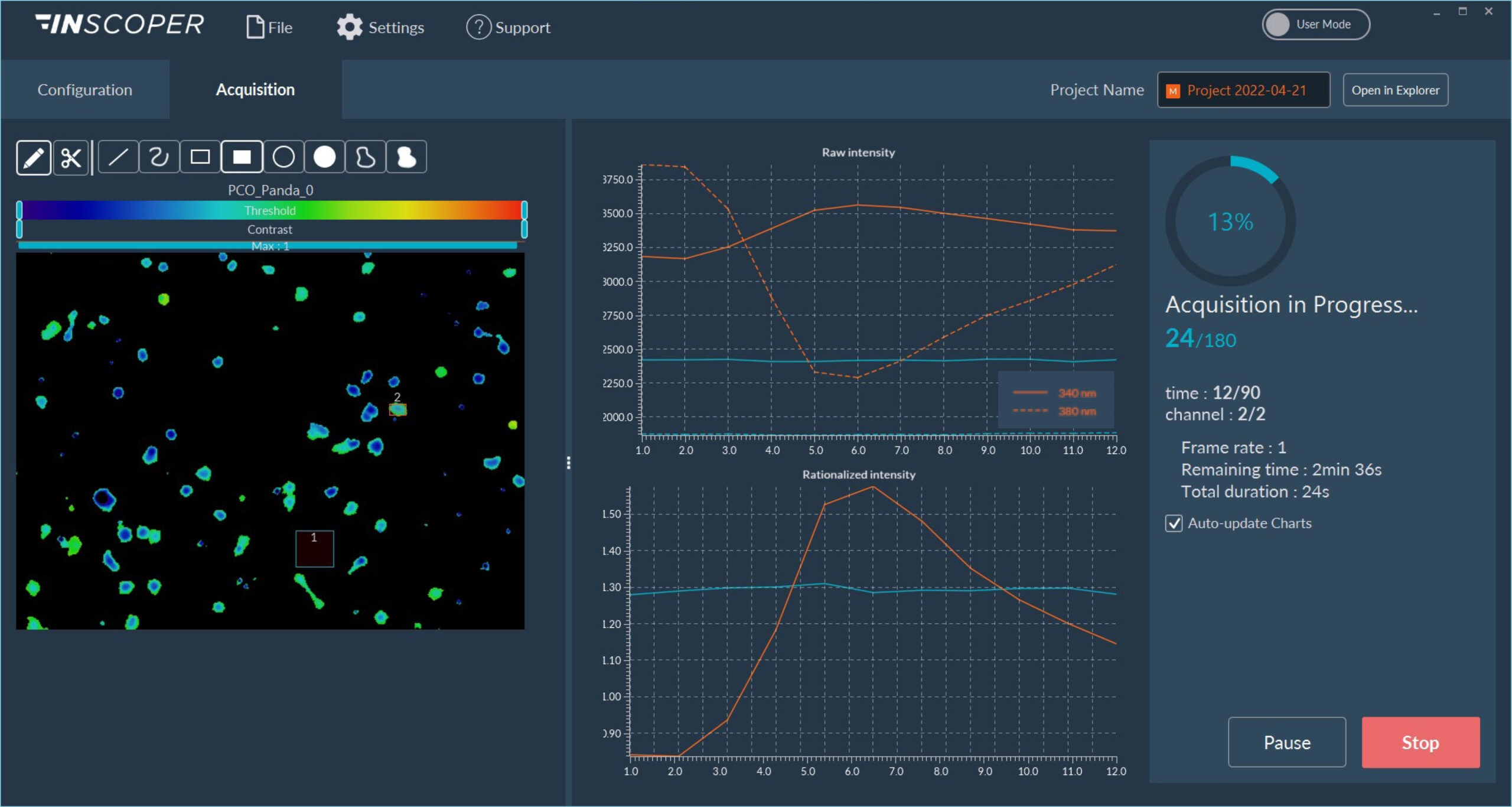
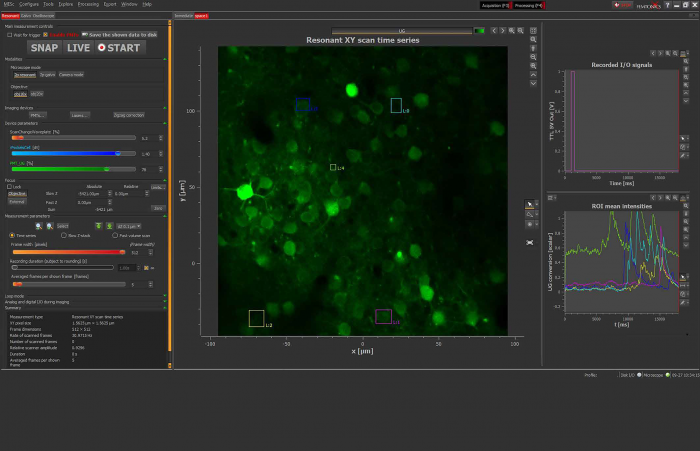
Рисунок 1: Интерфейс программного обеспечения Inscoper
Обзор пользовательского интерфейса Inscoper, используемого для визуализации последовательности сбора данных. Клетки были помечены Fura-2. Изображения можно наблюдать с помощью LUT, предназначенной для ратиометрической визуализации. Большая панель форм доступна для выбора ROIs (Regions Of Interests). Эти области будут использоваться для наблюдения за эволюцией необработанного и рационализированного сигнала флуоресценции. Все сгенерированные данные могут быть экспортированы в форматах .tif для изображений, .csv для графики и .avi для видео. Метаданные привязаны к каждому изображению.
Включая специально разработанный электронный блок для управления стойкой микроскопа и сторонними устройствами, Inscoper liveRATIO обеспечивает новый пользовательский опыт для ратиометрических приложений с улучшенными техническими характеристиками, полной системной интеграцией и простотой использования. Ядро технологии Inscoper устраняет любые программные задержки при управлении всей системой микроскопии. По сравнению с традиционными подходами, это увеличивает временное разрешение, что является основным преимуществом для применения в визуализации живых клеток. Помимо управления различными моторизованными элементами системы, Inscoper liveRATIO предлагает исследователям элегантный и полнофункциональный графический интерфейс для наблюдения за эволюцией флуоресцентных сигналов в биологических образцах благодаря обработке изображений в режиме реального времени (рис. 2). Inscoper liveRATIO - это новое современное решение для экспериментов FRET и ратиометрической визуализации (мониторинг концентрации ионов, измерение внутриклеточного рН, ...) с использованием флуоресцентных зондов.

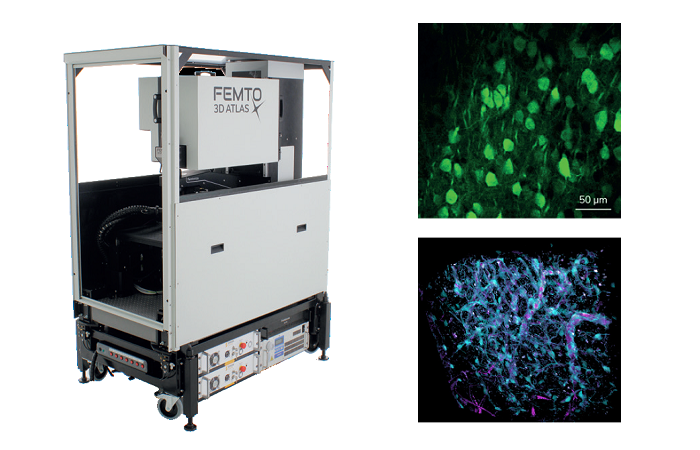
Рисунок 2: Экспериментальная установка для ратиометрической визуализации кальция, оснащенная Inscoper liveRATIO
Ратиометрическая визуализация кальциевых переходных процессов
Цели
Цель эксперимента охарактеризовать активацию γδ Т-клеток после презентации фосфоантигена. Для этого будут проводиться наблюдения за кальциевыми переходными процессами в лимфоцитах.
Материал
Этот эксперимент был проведен в сотрудничестве с микроскопическим центром MicroPICell (Нант, Франция). Был использован микроскоп Leica DMI 6000B (Leica, Wetzlar, Германия) с объективом HC Plan Apo 20x 0.70 NA (506166; Leica) (рис. 2). Для этого эксперимента камера была цифровой CMOS Orca Flash 4.0 (C11440; Hamamatsu Photonics, Hamamatsu, Япония), а световой источник - от CoolLED (pE-800fura; CoolLED, Andover, Великобритания). Управление микроскопом, получение и обработка изображений в реальном времени осуществлялись с помощью программы Inscoper liveRATIO (INSCOPER, Кессон-Севинье, Франция).
Метод
γδ Т-клетки были помечены Fura-2 AM (F1201; Thermofisher, Waktham, MA, USA), флуоресцентным зондом с высоким сродством к свободному внутриклеточному кальцию. Его спектральные свойства в присутствии низких концентраций кальция (максимум возбуждения = 362 нм, максимум эмиссии = 512 нм) отличаются от таковых в условиях высокого содержания кальция (максимум возбуждения = 335 нм, максимум эмиссии = 505 нм). Возбуждение при 340 нм и 380 нм позволяет соответственно получать изображения с кальций-связанными и свободными флуоресцентными зондами. Во время получения изображения в среду лимфоцитов вручную добавляли фосфо-антигены и наблюдали за флуоресценцией. Тот же эксперимент был проведен с использованием ДМСО (использованного для разведения Fura-2) в качестве отрицательного контроля.
Результаты
Для визуализации кальция используется множество красителей в соответствии с их свойствами (способность связывать кальций или пассивно диффундировать через плазматическую мембрану, длина волны возбуждения/испускания, интенсивность, яркость и стабильность). Кроме того, визуализация может быть выполнена с использованием нератиометрических (более удобных и быстрых, но не подходящих для количественной оценки) или ратиометрических методов (более сложных, но полностью приспособленных для количественных измерений).
В данном эксперименте предпочтение было отдано Fura-2 AM из-за (i) его ратиометрических свойств и (ii) его способности диффундировать через плазматические мембраны. Вкратце, Fura-2 AM необходимо последовательно возбуждать двумя различными длинами волн: 340 (со связанным кальцием) и 380 нм (свободный) с единственной эмиссией при 510 нм. Оба сигнала рационально использовать для количественной оценки. В базальных условиях концентрация внутриклеточного кальция оставалась низкой во всех покоящихся лимфоцитах. При добавлении ДМСО или фосфоантигенов (PA) в клеточную среду наблюдалось незначительное и преходящее увеличение соотношения 340/380. В Т-клетках, обработанных ДМСО, не наблюдалось изменений соотношения 340/380 в течение всего эксперимента. Однако лимфоциты, обработанные ПА, быстро демонстрировали увеличение этого соотношения, как показано на двумерных изображениях, графиках поверхности (Рисунок 3A) или на кимограммах (Рисунок 3B). Измерение сигнала 340/380 показало увеличение этого соотношения на 32,71 ± 0,07 % в клетках, обработанных ПА, несмотря на то, что в клетках, обработанных ДМСО, это соотношение оставалось стабильным (рис. 3C). Эти результаты подтвердили активацию γδ Т-клеток после стимуляции ПА.
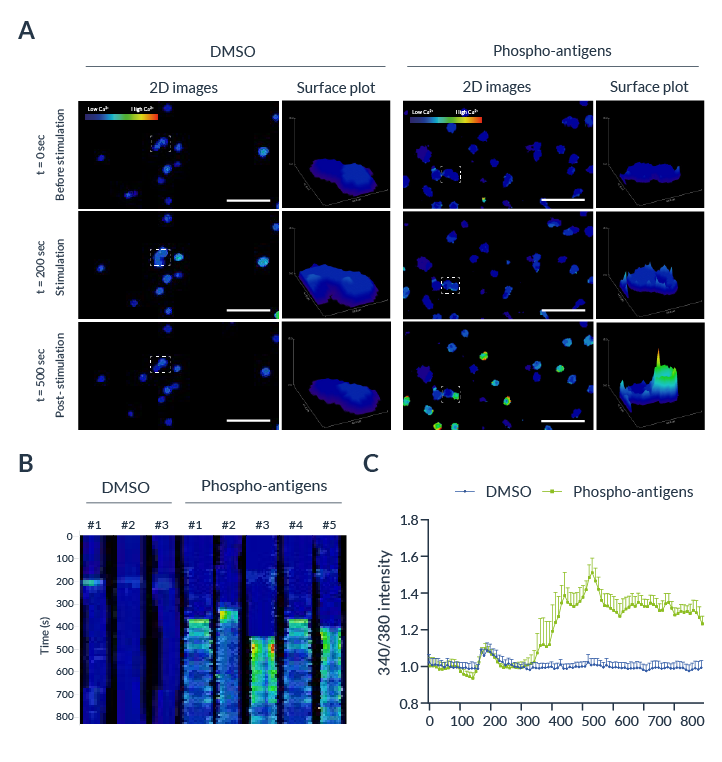
Рисунок 3: Активация Т-клеток, отслеживаемая с помощью ратиометрической визуализации с помощью Inscoper liveRATIO
(A) Репрезентативные изображения γδ Т-клеток, меченных Fura-2, при стимуляции ДМСО или фосфо-антигеном (PA). Графики поверхностей получены из каждого пунктирного квадрата. Масштабная линейка = 100 мкм. (B) Кимограмма, представляющая эволюцию интенсивности флуоресценции в зависимости от времени. Черная стрелка обозначает добавление ДМСО или ПА в среду. (C) Колебания кальция, индуцированные ДМСО или фосфо-антигеном на γδ Т-лимфоцитах, меченных Fura-2. Черная стрелка указывает на добавление ДМСО или ПА в среду. Данные выражены как среднее ± SEM.
Резюме
Inscoper liveRATIO предлагает биологам и пользователям видеомикроскопов возможность охарактеризовать активацию иммунных клеток, меченных Fura 2, после стимуляции. Это решение является идеальным инструментом для ратиометрической (концентрация ионов, измерение pH) и FRET (белок-белковые взаимодействия) визуализации на широком спектре биологических образцов. Обработка в реальном времени позволяет наблюдать все динамические изменения, которые могут происходить во время сеансов визуализации, с оптимизированным пространственно-временным разрешением. Помимо программного обеспечения для получения и обработки изображений, Inscoper liveRATIO может управлять всеми устройствами микроскопической системы для объединения многомерных и сложных исследований, включая настройки температуры и CO2 в камере инкубатора или шприцевых насосов для микрофлюидных экспериментов. Следующим усовершенствованием для приложений ратиометрической визуализации будет отслеживание клеток для мониторинга флуоресценции в реальном времени без влияния подвижности клеток.