Международная армия нейробиологов пытается лучше понять внутреннюю работу мозга, исследуя корреляции между нейронной активностью и поведением свободно движущихся или частично сдерживаемых лабораторных животных. Наилучшим методом контроля нейронной активности, активации или выключения опсин-экспрессирующих нейронов является оптогенетика. Распространенными оптическими методами для мониторинга нейронной активности меченных флуорофором нейронов являются волоконная фотометрия и флуоресцентная микроскопия непосредственно на голове исследуемого животного.
Нейробиологи, по-видимому, в равной степени разделены во мнении по поводу того, является ли волоконная фотометрия или флуоресцентная микроскопия более подходящим методом мониторинга нервной активности, выявленной при возбуждении определенных флуорофоров. Но нет такого разделения относительно оптогенетики и ее контроля над нейронной активностью с помощью света и оптики.

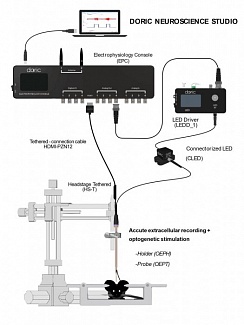
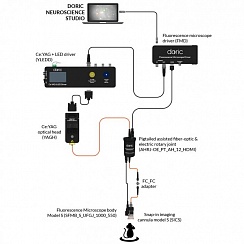
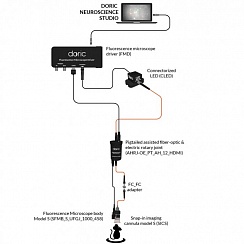
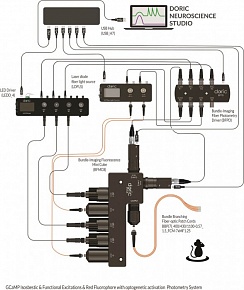
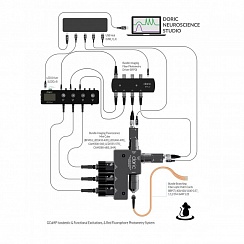
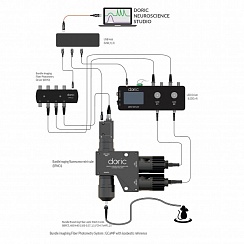
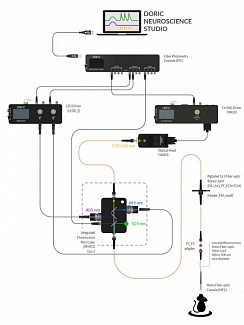
Рисунок 1. Типовая фотометрическая система. Предоставлено Doric Lenses
В оптогенетике используется свет, чтобы активировать или деактивировать клетки, помеченные генетически кодируемыми светочувствительными белками или опсинами, которые связаны с ионными каналами. Когда светозависимый ионный канал поглощает свет определенного диапазона длин волн, он меняет свою конфигурацию и позволяет ионам поступать в клетку, модулируя ее активность. Экспрессируя опсины в определенной популяции клеток, эти клетки становятся чувствительными к световым сигналам и могут управляться светом.
Наиболее популярными опсинами являются канал родопсин-2 (ChR2) и халордопсин-3.0 (NpHR3.0). Когда синий свет (диапазон длин волн от 450 до 473 нм) активирует ChR2, открывается неспецифический проницаемый для катионов канал, и происходит деполяризация клетки. Светозависимый хлоридный насос NpHR3.0 активируется желтым светом (длина волны 595 нм), позволяя хлорид-ионам проникать в клетку, вызывая гиперполяризацию нейрона или его выключение. Порог мощности света активации опсина составляет несколько мВт/мм² для синего и до 20 мВт/мм² для желтого света.
Прямое измерение нервной электрической активности у свободно движущихся животных очень сложный процесс из-за временных ограничений и низкой чувствительности доступных на рынке датчиков. По этим причинам выгодно использовать косвенный подход.
Колебания кальция на клеточном уровне связаны с основной электрической активностью и могут быть измерены с использованием флуоресцентных генетически кодированных индикаторов кальция (GECI). Изменения флуоресценции указывают на изменение концентрации кальция, выявляя клеточную активность.
С помощью GECI можно ориентироваться на определенный тип клеточной связи. Наиболее распространенным GECI является GCaMP, белок, который поглощает синий свет с пиком поглощения около 495 нм и излучает зеленый свет с пиком излучения около 510 нм. Флуоресцентная эмиссия индикатора GCaMP гасится, когда кальций отсутствует, и увеличивается с увеличением концентрации кальция.
Волоконная фотометрия
Для мониторинга нейронной активности у свободно движущихся животных с помощью волоконной фотометрии постоянно имплантированное оптическое волокно доставляет возбуждающий свет к нейронам помеченным флуоресцентным индикатором (индикаторами) кальция и собирает общую флуоресценцию, вызванную активностью. Диаметр световода, передающего и собирающего свет волокна, обычно составляет 200 или 400 мкм. Небольшой размер имплантата позволяет использовать волоконную фотометрию для записи из нескольких областей мозга исследуемого животного.
Волоконная фотометрия совместима с многоцветными и даже FRET (флуоресцентным резонансным переносом энергии) экспериментами. Базовая экспериментальная установка состоит из флуоресцентного куба, который разделяет свет возбуждения и излучения, фотоприемника, который измеряет изменение флуоресценции и блока сбора данных, который регистрирует электрический сигнал, поступающий от фотоприемника. Более чувствительные фотоприемники требуют менее интенсивного света возбуждения, уменьшая фотообесцвечивание и фотоповреждение в ткани.
Однако интеграция всей флуоресценции одного немодулированного возбуждения с помощью одного детектора делает невозможным отличить изменения флуоресценции, исходящие от индикатора кальция от изменений, вызванных нестабильностью интенсивности света возбуждения, изменениями оптической связи вращающегося волоконного соединителя и движениями мозга.
Отделение реальных изменений кальция от этих артефактов возможно, если свет возбуждения модулируется или если одновременно используется другая длина волны возбуждения, не зависящая от кальция.
При выборе компонентов для установки волоконной фотометрии выберите стабильный источник света, который можно модулировать, оптимизированное вращающееся соединение, минимизирующее колебания при вращении, малошумящий фотодетектор с усилителем, оптоволоконные кабели и канюли с низкой автофлуоресценцией. Флуоресцентные кубы, состыкованные с волоконным световодом, предотвращают утечку света и устраняют конечному пользователю проблему оптического выравнивания.
Разным применениям требуются кубы с соответствующим количеством портов и внутренней конфигурацией. Аппаратное и программное обеспечение для сбора данных упрощает настройку сеансов записи волоконно-фотометрических данных с различными параметрами для возможностей возбуждения и синхронной регистрации сигнала (рисунок 1).
Микроскопия. Установка системы на голове
Миниатюрная система для флуоресцентной микроскопии на голове исследуемого животного позволяет получать изображения с микронным разрешением вспышек активности кальция в меченных GECI нейронах, которые возбуждаются светом в мозге свободно движущегося животного.
Типовой подход к миниатюрным флуоресцентным микроскопам с креплением на голове исследуемого животного заключается в использовании миниатюрного CMOS-сенсора в качестве датчика изображения, светодиодного источника света, дихроичного фильтра внутри корпуса микроскопа и ретрансляционной линзы с градиентным показателем преломления (GRIN-линза) в имплантированной в голову животного канюле для формирования изображения. Электронный сигнал от датчика изображения затем электрически отправляется на блок сбора данных и компьютер пользователя.
Однако компания Doric Lenses использует внешние источники света, которые подключены к микроскопу через оптическое волокно и вспомогательное электрооптическое вращающееся соединение. Это повышает шансы найти подходящий источник света - светодиод, лазер или другой источник света - с соответствующим спектральным диапазоном и необходимым уровнем оптической мощности. В случае встроенных источников света единственными подходящими миниатюрными источниками света являются светодиоды, но они не охватывают все спектральные полосы, могут не иметь достаточной оптической мощности и не могут быть легко заменены.

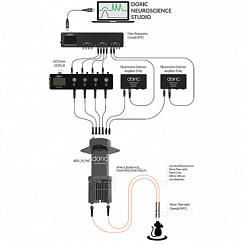
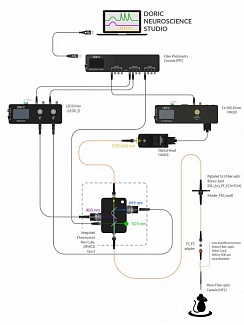
Рисунок 2. Корпус двухцветного миниатюрного микроскопа. Предоставлено Doric Lenses.
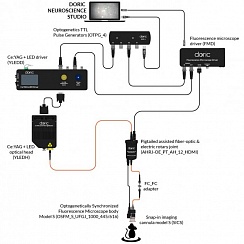
Подход компании Doric Lenses имеет дополнительные преимущества, когда используются два или более цветов света, как в оптогенетически синхронизированном флуоресцентном микроскопе, который сочетает в себе возбуждение флуоресценции и оптогенетическую стимуляцию, или как в двухцветном микроскопе, который наблюдает активность кальция в двух группах нейронов, меченных разными GECI.
Сильное поглощение и рассеивание света внутри мозговой ткани ограничивает глубину получения изображения приблизительно до 150 микрон. По этой причине промежуточная линза должна быть расположена как можно ближе к области интереса. Чтобы минимизировать повреждение мозга постоянно имплантированная линза должна быть максимально тонкой. Для сбора флуоресценции линза должна иметь большую числовую апертуру. Пока что кажется, что только GRIN линза является приемлемым вариантом.
Однако GRIN линзы страдают от высокой хроматической аберрации, которая не может быть легко компенсирована. В своем двухцветном флуоресцентном микроскопе компания Doric Lenses компенсирует этот хроматический сдвиг, используя два CMOS-сенсора и отдельные оптические пути для сигналов изображения, получаемых из одной оптической плоскости (рис. 2).
Требуемая мощность освещения для оптогенетической стимуляции примерно в 10 раз больше, чем мощность необходимая для возбуждения флуоресценции, предпочтительно без каких-либо перекрестных помех. Это требует тонко настроенных оптических фильтров и соответствующего управления рассеянным светом, чтобы предотвратить стимуляцию опсина при записи флуоресцентного изображения.
Оборудование, которое имеет значение
Как для волоконной фотометрии, так и для флуоресцентной микроскопии, при установке системы на голове исследуемого животного, требуется оптическая и/или электрическая связь и оптический порт входа (волоконно-оптический световод или визуализирующая канюля) постоянно имплантированные в голову животного.
Оптический световод состоит из оптоволоконного кабеля с гибкой оплеткой. Оплетка защищает шнур от пережевывания, и его прочность в значительной степени зависит от размера и возраста лабораторного животного и типа проводимых поведенческих экспериментов.
Многомодовые волокна толстого сечения с большой числовой апертурой (NA) предпочтительны для самого оптоволоконного кабеля, потому что они обеспечивают более высокую мощность подачи света из светодиодного осветителя и лучший сбор флуоресценции ткани. Когда в качестве источника света используются лазерные диоды для некоторых оптических вращающихся соединений лучше подходят волокна меньшего сечения и большей числовой апертуры NA.

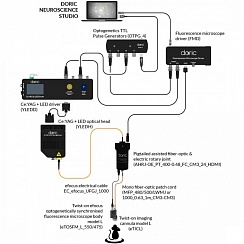
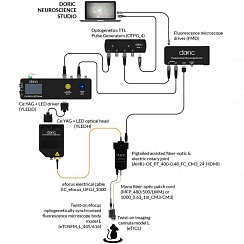
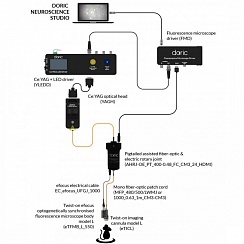
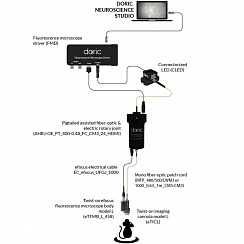
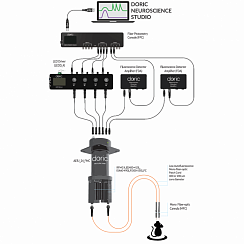
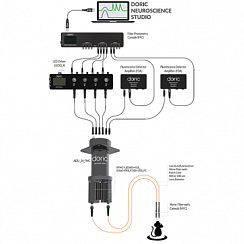
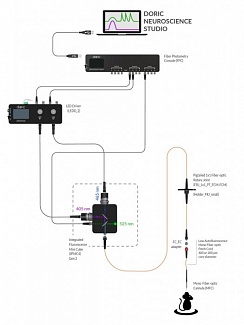
Рисунок 3. Двухцветная оптогенетическая стимуляция с помощью источника света Ce: YAG и LED. Предоставлено Doric Lenses
Часть канюли, прикрепленная к верхней части черепа, представляет собой просто оптический разъем, хотя и очень маленький, в то время как сторона, обращенная к внутренней части мозга, имеет заданную длину оптического волокна или стержневую линзу, направленную к выбранной области интереса. Рассеяние света в ткани мозга требует, чтобы кончик волокна был как можно ближе к исследуемой области. Канюли могут быть выполнены в различных формах, они обеспечивают точное наведение во время имплантации и создают постоянное и прочное соединение с оптоволоконным кабелем.
После того, как кончик волокна канюли расположен рядом с группой нейронов, помеченных флуорофорами или фоточувствительными опсинами, нейронную активность можно активировать или деактивировать с помощью оптогенетики и контролировать с помощью волоконной фотометрии или флуоресцентной микроскопии.
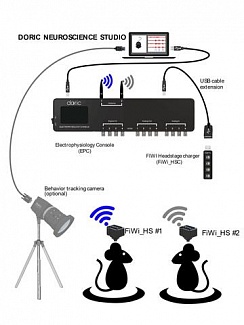
Объединив внешнюю камеру для записи поведения животного, некоторые модулированные источники света с их драйверами, оптоволоконное поворотное соединение, связку оптоволоконных кабелей, соответствующие детекторы и консоль для синхронизации всего этого оборудования, можно проводить простые эксперименты по исследованию поведения животного.
Все может стать более сложным, если группы нейронов помечены разными флуорофорами или опсинами и освещаются соответствующими импульсами возбуждения или активации. В этом случае автофлуоресценция вычитается из сигнала, и осуществляется флуоресцентная резонансная передача энергии или FRET.
С точки зрения фотоники все это стало возможным благодаря крайней миниатюризации всех задействованных компонентов, особенно тех, которые установлены на черепе животного.
Компания Doric Lenses была вовлечена в исследования, связанные с нейробиологией, когда лаборатория Карла Диссерота в Стэнфордском университете запросила изготовить волоконно-оптическое вращающееся соединение для своих экспериментов по оптогенетике со свободно движущимися оптически привязанными мышами. Это привело к созданию миниатюрного поворотного соединения с низким коэффициентом трения и коннектором для подключения оптоволоконного кабеля.
Быстрый успех использования вращающихся соединений привел к осознанию того факта, что оптогенетика нуждается в полной фотонной инфраструктуре от модулированного источника света до постоянных имплантатов в головной мозг животных. В последствии были разработаны важные инструменты и компоненты для оптогенетики, в том числе одно- и двухволоконная оптическая канюля, ряд оптических и гибридных поворотных соединений с низким коэффициентом трения, оптоволоконные источники света, включая мощные источники желтого света и различные оптоволоконные кабели.
Управление мозговой активностью с помощью оптогенетики и наблюдение за изменениями в поведении - это первый шаг к пониманию связей между ними. Чтобы лучше понять основную сложность мозга, важно также контролировать его активность на клеточном уровне. Разработка оборудования для оптогенетики подготовила почву для осуществления оптического мониторинга нейронной активности с помощью волоконной фотометрии или флуоресцентной микроскопии.