Эксперименты по взаимодействию белков методом резонанса Фёрстера (FRET)
Передача энергии резонанса Фёрстера (FRET- Förster resonance energy transfer) представляет собой взаимодействие двух молекул, в котором полоса излучения одной молекулы перекрывает полосу поглощения другой. В этом случае энергия от первой молекулы, донора, может перейти во вторую, акцептор. FRET может привести к чрезвычайно эффективному гашению флуоресценции донора и, следовательно, к значительному уменьшению времени жизни донора. Скорость передачи энергии от донора к акцептору уменьшается с шестой степенью расстояния. Поэтому это заметно только на расстояниях менее 10 нм. FRET используется в качестве инструмента для исследования межбелкового взаимодействия. Различные белки помечены донором и акцептором, и FRET используется в качестве индикатора связывания между этими белками. FRET является наиболее частым применением метода FLIM.
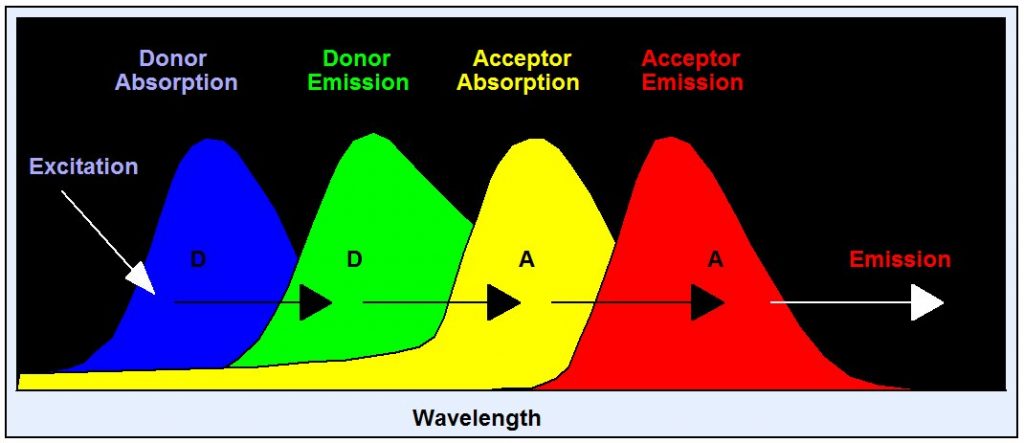
Рис. 1. Принцип передачи энергии резонанса Фёрстера (FRET)
Из-за своей зависимости от расстояния метод FRET стал важным инструментом клеточной биологии. Различные белки помечаются донором и акцептором, затем метод FRET используется для проверки того, являются ли белки физически связанными и для определения расстояний в нанометровом масштабе.
Одноэкспоненциальная интерпретация данных FLIM-FRET
Интерпретация данных FLIM-FRET проста: при отсутствии FRET время жизни донора не изменяется. Когда FRET присутствует, донор теряет свою энергию возбуждения в акцепторе, и время жизни уменьшается, смотрите рисунок ниже.
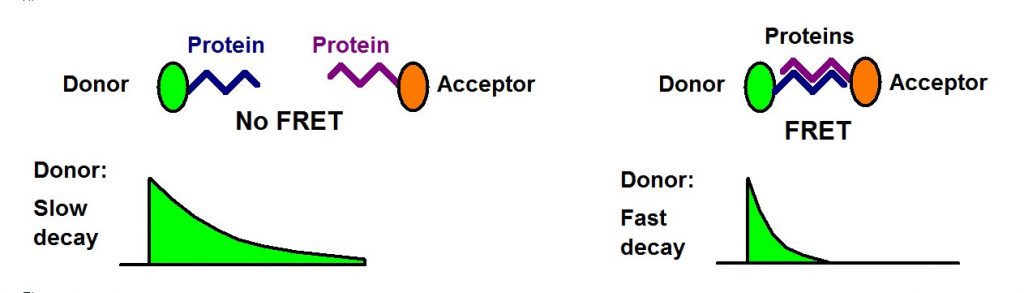
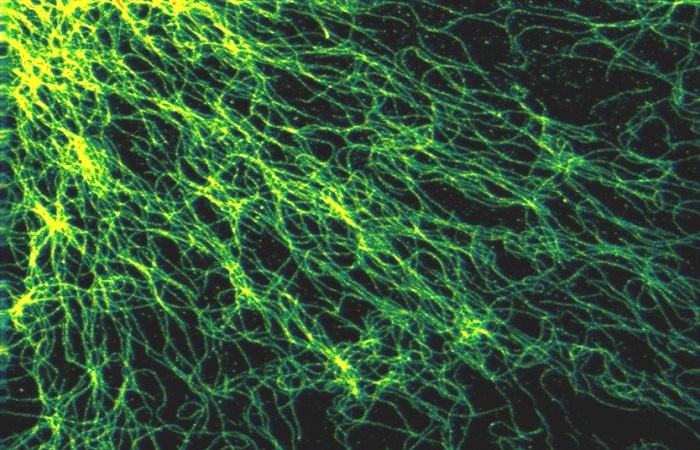
Рис. 2. Эксперимент по взаимодействию белков FRET. Когда белки взаимодействуют, происходит FRET, и время жизни флуоресценции донора уменьшается.
Использование FLIM для FRET имеет очевидное преимущество, заключающееся в том, что интенсивность FRET получается из одного изображения времени жизни донора. Когда происходит FRET, время жизни флуоресценции донора уменьшается, когда FRET отсутствует, оно остается постоянным. Все, что необходимо для обнаружения белкового взаимодействия - это изображение времени жизни донора. Поэтому донорское протекание и непосредственно возбужденная акцепторная флуоресценция не влияют на измерения FLIM-FRET. Пример показан на рисунке ниже.
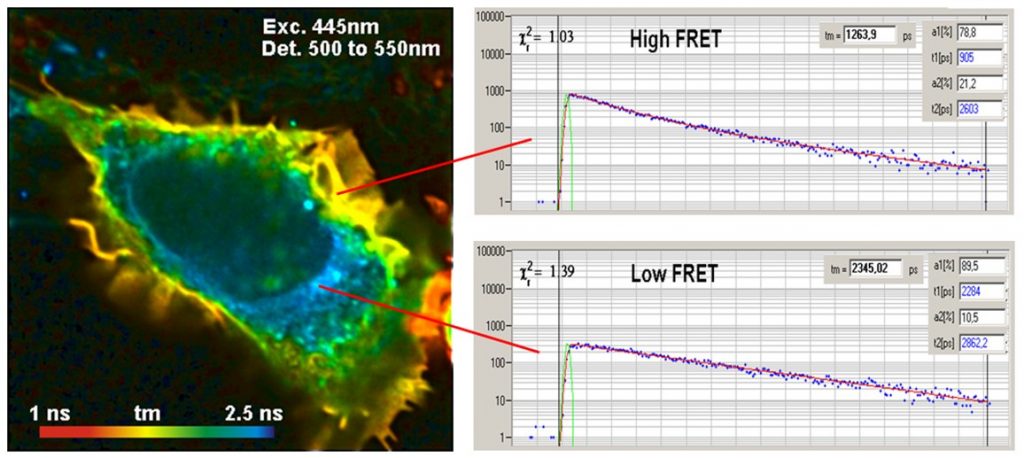
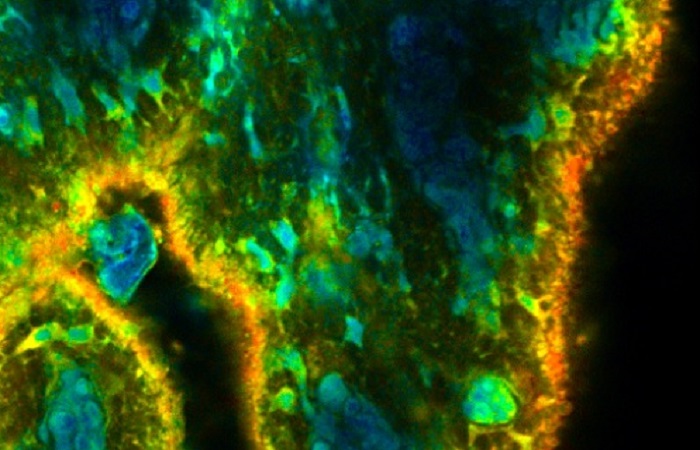
Рис. 3. FRET Изображение клетки, которая имеет взаимодействующие белки в клеточной мембране.
Двойной экспоненциальный FLIM-FRET анализ
Во всех экспериментах по взаимодействию с белками обычно существует смесь взаимодействующих и не взаимодействующих белков. Как доля взаимодействующих белков, так и расстояние между белками влияют на чистую эффективность FRET, полученную из интенсивностей флуоресценции. Поэтому нельзя сказать, связано ли изменение эффективности FRET с изменением расстояния или с изменением доли взаимодействующих белков.
TCSPC FLIM решает проблему взаимодействия и невзаимодействия донора с помощью двойного экспоненциального анализа времени жизни. Получающиеся донорные функции распада могут быть аппроксимированы двойной экспоненциальной моделью с быстрой составляющей от взаимодействующих донорных молекул и медленной составляющей времени жизни от не взаимодействующих донорных молекул. Есть несколько причин, по которым донор не взаимодействует. Белок может просто не быть связан друг с другом, акцепторный белок не может быть помечен акцептором, или ориентация между донором и акцептором может быть неправильной. Ориентация обычно считается случайной и учитывается фактором k2. Если маркировка завершена, как и следовало ожидать, если клетка экспрессирует слитые белки вариантов GFP, компоненты распада представляют собой фракции взаимодействующих и не взаимодействующих донорных молекул. Амплитуды a и b, скорректированные на k2, представляют собой доли взаимодействующих и не взаимодействующих белковых молекул. Состав донорной функции распада показан на рисунке ниже.
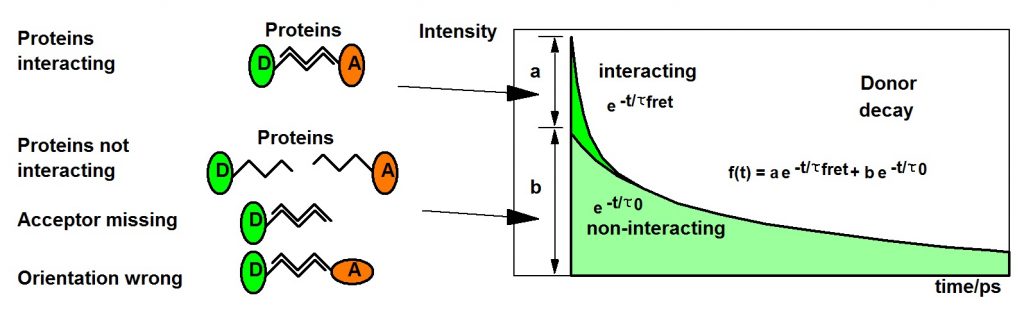
Рис. 4. Смесь взаимодействующих и не взаимодействующих белков обеспечивает функцию двойного экспоненциального донорного распада. Двойной экспоненциальный анализ распада разделяет взаимодействующие и не взаимодействующие донорные фракции.
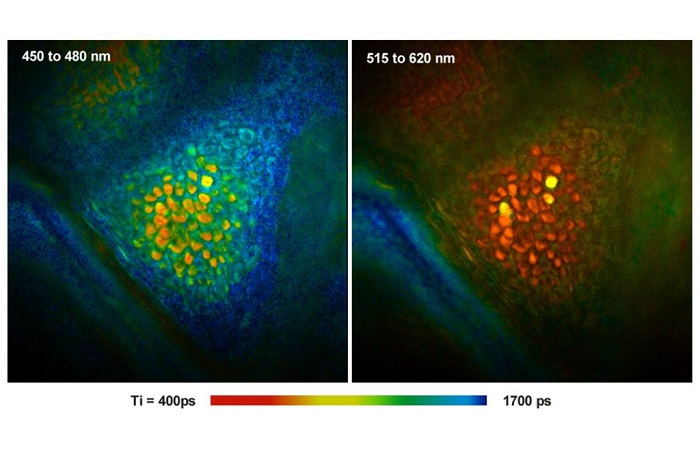
На следующем рисунке показан результат двойного экспоненциального анализа FLIM-FRET. На левом изображении показано отношение времен жизни невзаимодействующих и взаимодействующих донорных фракций t0/tfret. Распределение t0/tfret в разных областях показано слева. Расположение максимумов отличается только на 10%, что соответствует изменению расстояния около 2%. Однако изменение коэффициентов интенсивности a/b и, следовательно, в отношении взаимодействующих белков Nfret/N0 составляет около 10:1.
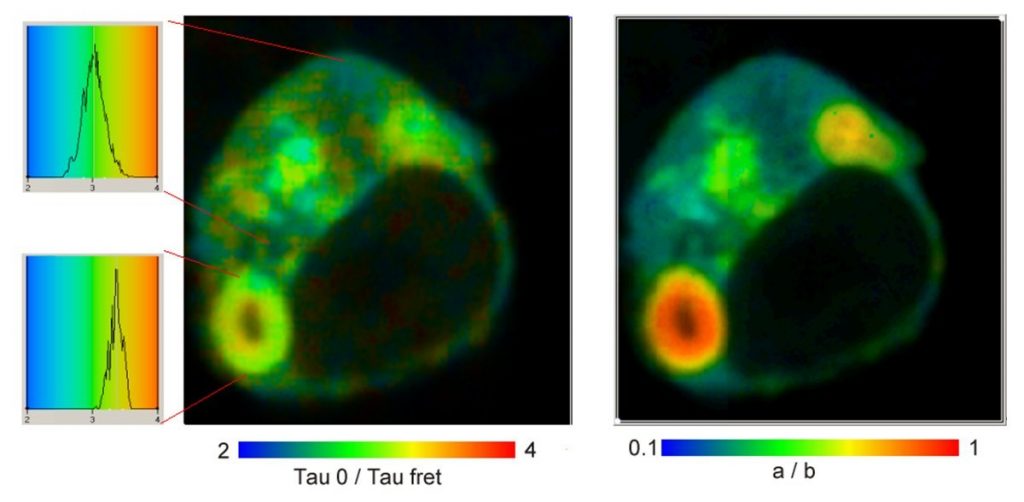
Рис. 5. Двойной экспоненциальный анализ FRET. Слева: соотношение продолжительности времени жизни не взаимодействующего и взаимодействующего донора. Справа: соотношение количества взаимодействующих и не взаимодействующих доноров.
Результат ясно показывает, что изменение времени жизни с одной экспонентой почти полностью обусловлено изменением доли взаимодействующих белков, а не изменением расстояния между донором и акцептором. Другими словами, интерпретация вариаций времени жизни с одной экспонентой (или классической эффективности FRET из стационарных экспериментов!) как вариаций расстояния приводит к неверным выводам. Поэтому двойной экспоненциальный анализ FRET является существенным шагом к количественным экспериментам FRET.