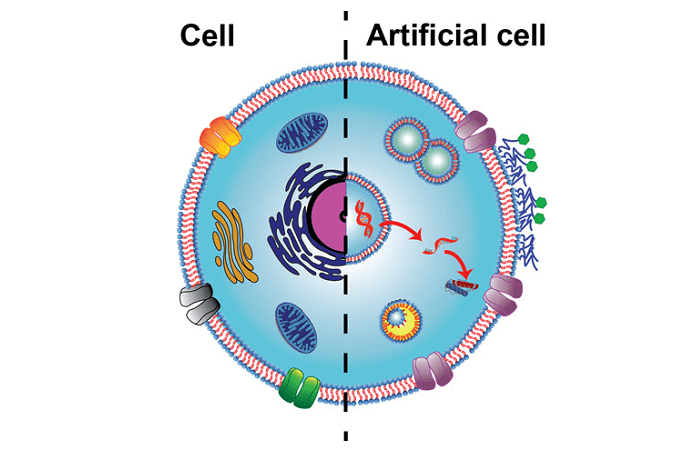
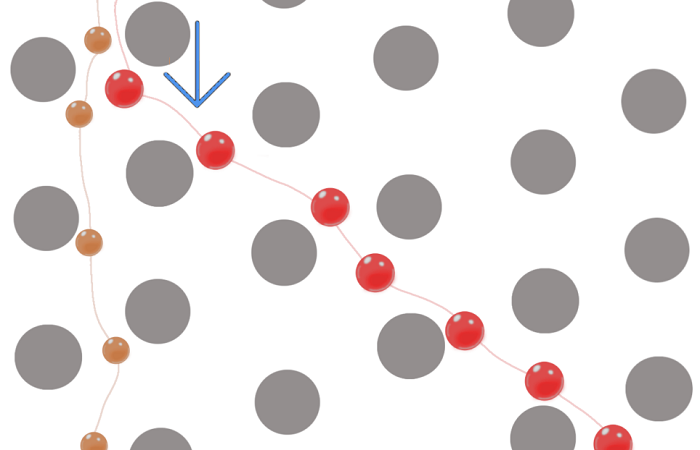
В статье, опубликованной в 2020 году в журнале Cell, Мишель М. Нава и Екатерина А. Мирошникова из группы Сары А. Викстрем в Хельсинки с соавторами демонстрируют способность ядра, клеток и тканей быстро адаптироваться к механическому стрессу и избегать повреждения ДНК. Целостность генома сохраняется с помощью двух независимых механизмов. Во-первых, быстрая защита ДНК обеспечивается за счет преходящего размягчения ядра независимо от известных клеточных механосенсоров. Во-вторых, долгосрочные воздействия смягчаются благодаря перестройке тканей для наилучшего восприятия механической нагрузки.

Группа Сары А. Викстрём в Хельсинки
Аннотация: Ткани защищают свою ДНК при механических нагрузках
Весьма примечательной особенностью наших тканей и клеток является их способность выдерживать механические нагрузки в повседневной жизни. Любое растяжение, вытягивание или сжатие потенциально может привести к разрыву клеток и тканей и повреждению ДНК, но такие повреждения встречаются редко. В связи с этим возникает вопрос: каковы механизмы, защищающие наш геном и клетки от подобных внешних воздействий?
Механизмы защиты ДНК в ответ на механическое воздействие недавно были глубоко изучены группой Сары Викстрём из Хельсинкского института наук о жизни и Исследовательского института Вихури при Хельсинкском университете. Используя ряд биомеханических и микрофлюидных реакторов, позволяющих имитировать растяжение и сжатие in vivo, авторы показывают, как клетки и ткани образуют два биологически и временно различных механизма, обеспечивающих защиту ДНК и сохранение целостности генома.
Введение
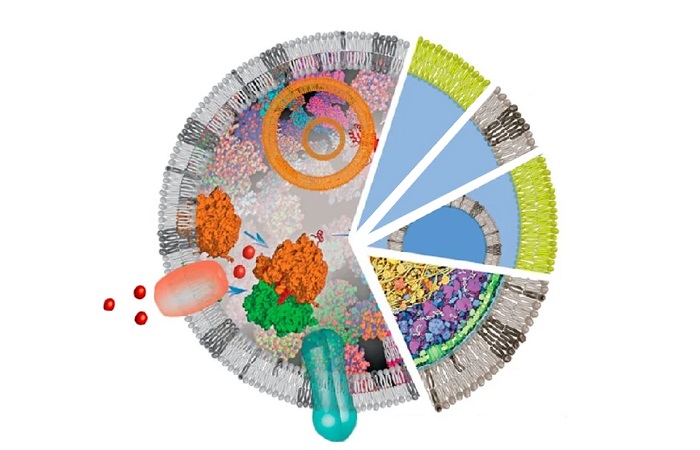
Все клетки и ткани реагируют на механическое воздействие не одинаково. Например, известно, что раковые клетки при механической деформации сильно повреждают ДНК, в то время как эпителиальные ткани образуют прочные физические барьеры против внешних сил. Внутри клеток ДНК изолирована и защищена от остальной части клетки двойной липидной бислойной структурой - ядерной оболочкой. На внутренней ядерной мембране волокнистые белки ядерного ламинина поддерживают форму и структуру ядра. Важно отметить, что ядерная оболочка и ее компоненты служат центром для компонентов цитоскелета клетки, которые сами направляют механически индуцированные внешние напряжения.
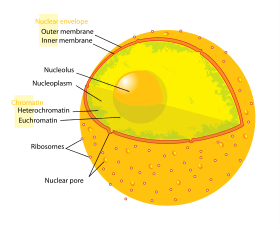
Рис. 1 Структура ядра человека
Внутри ядра ДНК динамически конденсируется в эухроматин (транскрипционно активный и низкой плотности) и гетерохроматин, соответственно с низким и высоким уровнем конденсации двухцепочечной ДНК. Что важно в контексте данного исследования, плотные участки ДНК гетерохроматина связаны с пластинкой. В то время как о механическом воздействии микросреды сообщалось в литературе, механизмы, объясняющие, как хроматин реагирует и как клетки рассеивают такие силы, недостаточно хорошо изучены. Используя микрофлюидику для имитации физиологического состояния клеток, Нава, Мирошникова и соавторы демонстрируют, как клетки реагируют как в краткосрочной, так и в долгосрочной перспективе.
Методы: Микрофлюидное сжатие и растяжение клеток/тканей для имитации повреждения ДНК, вызванного механическим воздействием
"Было интересно понять, что мы можем изменять механические свойства хроматина, просто воздействуя на стволовые клетки механическими силами. Еще более поразительным было то, что если мы экспериментально предотвращали эти изменения в механике хроматина, то стволовые клетки теперь получали повреждения ДНК, что указывало на то, что мы открыли важный защитный механизм" – Екатерина Мирошникова, автор. К клеткам и тканям были приложены два типа механических сил, чтобы получить информацию о реакции на механические силы как на клеточном уровне (краткосрочный ответ), так и на уровне ткани (долгосрочная адаптация).
Ядерное сжатие
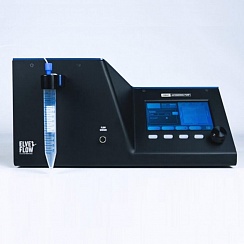
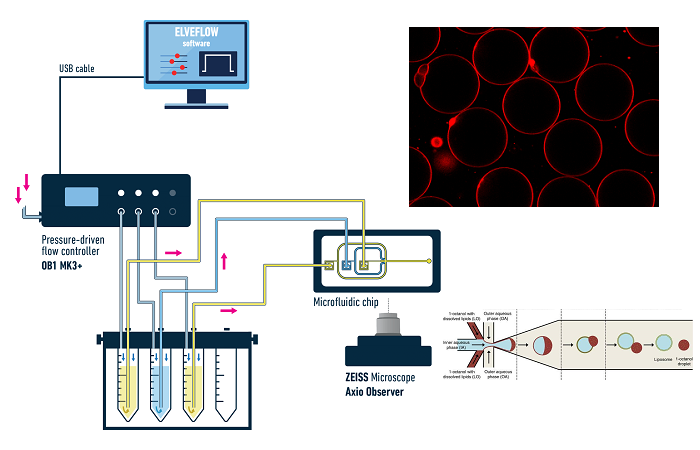
Для проведения этого эксперимента Нава, Мирошникова и соавторы выращивали эпидермис кожи или мезенхимальные стволовые клетки в микрофлюидной системе клеточного конфайнмента. Впервые эта система была опубликована Le Berre et al. в 2012 году и в настоящее время является коммерчески доступной (4Dcell, подразделение компании Elveflow). Он позволяет удерживать клетки в микрофлюидном канале и прикладывать контролируемые внешние силы с помощью генератора давления. Схема этого ограничителя, представленная компанией 4Dcell на своем сайте, показана на рисунке 2.
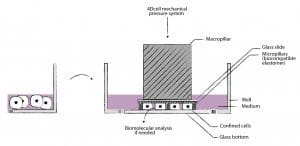
Рис. 2 Схема ограничителя от 4Dcell
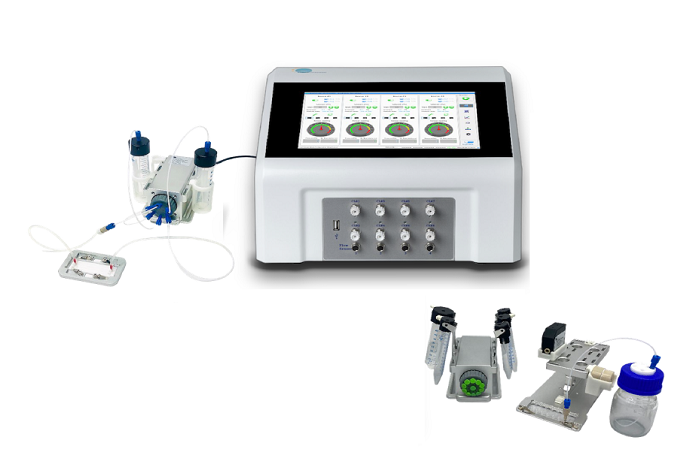
Мезенхимальные стволовые клетки или стволовые клетки эпидермиса кожи (CellInTec HPEKp // ATCC CRL-1629 // ATCC CCL-121) были посеяны в конфайнмент, и к клеткам применялись различные уровни сжатия благодаря двойному регулятору давления. Эта специфическая конфигурация Elveflow OB1 -900 мбар / 1000 мбар позволяла применять отрицательное давление и запускать компрессию.
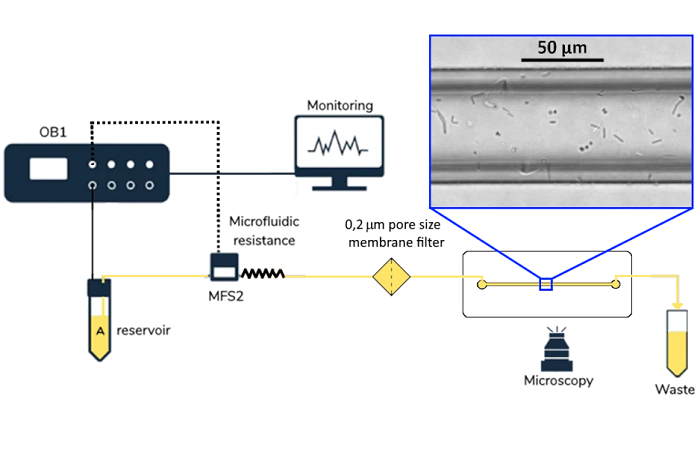
Как и умеренное одноосное растяжение от 20% до высоких 40%, 30%-ное сжатие с помощью конфайндера привело к ядерной деформации в виде уплощения ядер. Обе деформации вызвали кальций-зависимый гетерохроматиновый ответ H3K9me3. Авторы далее определили, что потеря H3K9me3 является движущей силой размягчения ядер и, следовательно, необходима для защиты от повреждений ДНК при механическом стрессе.

Рисунок 3: Микрофлюидная установка для анализа сжатия ядер
Растяжение клеток и тканей
Анализы на растяжение были проведены в соответствии с работами Faust et al. 2011 и Noethel et al. 2018. Этот изготовленный на заказ одноосный клеточный растяжитель основан на эластомерах PDMS площадью 4 см2, в которые можно посеять или прикрепить клетки и ткани, соответственно. Затем эластомеры зажимаются в специальных камерах, и вся система подвергается одноосному растяжению.
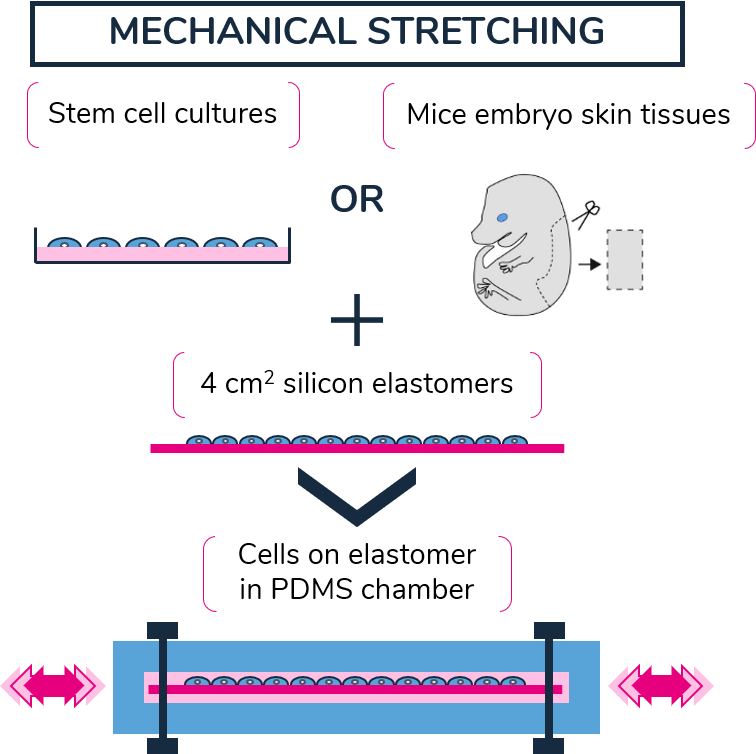
Рисунок 4: Камера и протокол для проведения анализов на растяжение
Основные выводы
Повреждение ДНК предотвращается в стволовых клетках посредством краткосрочного размягчения ядер и долгосрочной переориентации монослоя
Ядерная деформация (удлинение в случае растяжения, уплощение в случае сжатия) позволила глобально размягчить ядра за счет уменьшения количества периферического гетерохроматина. Преходящая потеря гетерохроматина не вызывала больших транскрипционных эффектов, поскольку изменения происходили в основном в некодирующих областях генома. Другими словами, ядра могут разумно реагировать на механические стрессы, изменяя свои физические свойства для предотвращения повреждения ДНК, сохраняя гомеостатическую транскрипционную активность и, таким образом, поддерживая базальное состояние клетки.
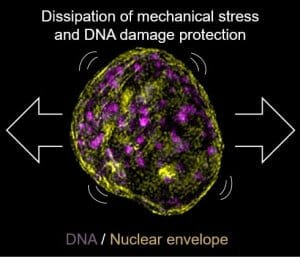
В целом, эти результаты показывают, что ядра быстро реагируют на механическое воздействие для предотвращения повреждения ДНК путем сокращения ламина-ассоциированного гетерохроматина на ядерной периферии вблизи ядерной оболочки. Этот ответ основан на ядерной деформации, вызванной высвобождением кальция из эндоплазматического ретикулума, который является непрерывным с внешней ядерной мембраной, являющейся частью ядерной оболочки. На более длительных временных интервалах ткани реагируют на механическое воздействие, переориентируя свой цитоскелет для рассеивания сил от клетки к клетке и одновременно восстанавливая базовый уровень гетерохроматина.
Нава, Мирошникова и их коллеги показали, что F-актин переориентируется перпендикулярно силам растягивающего напряжения, чтобы смягчить распространение механического напряжения от клетки к клетке. Этот надклеточный замедленный ответ опирается на контакты между клетками для предотвращения ядерного напряжения. Авторы подтвердили эту замедленную реакцию на тканевом уровне на эксплантатах кожи мышей.